进货单( 0 )
建议零售价: ¥91.00/瓶
亮健价:¥认证可见 / 瓶
通用名称: 丁苯酞软胶囊
生产厂家: 石药集团恩必普药业有限公司
批准文号: 国药准字H20050299
有效期:
是否拆零:是

甲泼尼龙片
津药和平 (天津) 制药有限公司 (曾用名:天津金耀药业有限公司)
4mg*24片(尤金)

阿司匹林肠溶片
石药集团欧意药业有限公司
100mg*36片
Q拉莫三嗪片
DELPHARM POZNAN SPOLKA AKCYJNA
50mg*30片

富马酸喹硫平片
阿斯利康制药有限公司
0.2g*20片(思瑞康)

盐酸贝尼地平片
协和麒麟(中国)制药有限公司分装
8mg*7片

复方甘草酸苷片
乐普药业股份有限公司
30片(帅能)

阿卡波糖片
北京福元医药股份有限公司
50mg*30片

复方牛胎肝提取物片
黑龙江江世药业有限公司
40mg*36片(安珐特)

复方甲氧那明胶囊
上海上药信谊药厂有限公司
40粒

果糖二磷酸钠口服溶液
北京华靳制药有限公司
(1g:10ml)*6支

舒洛地特软胶囊
ALFASIGMA S. p. A.
250LSU*12粒

葡萄糖酸锌片
海南制药厂有限公司
70mg*100片(南岛)

润洁萘敏维滴眼液
山东博士伦福瑞达制药有限公司
10ml(润洁)

螺内酯片
杭州民生药业股份有限公司
20mg*100片

利福平胶囊
沈阳红旗制药有限公司
0.15g*100粒













| 产品名称 | 恩必普 丁苯酞软胶囊 0.1g*24粒 |
| 产品规格 | 0.1g*24粒 |
| 生产企业 | 石药集团恩必普药业有限公司 |
| 批准文号 | 国药准字H20050299 |
| 性状 | 本品为软胶囊,内容物为淡黄色或黄色油状液体。 |
| 有效日期 | 1095 |
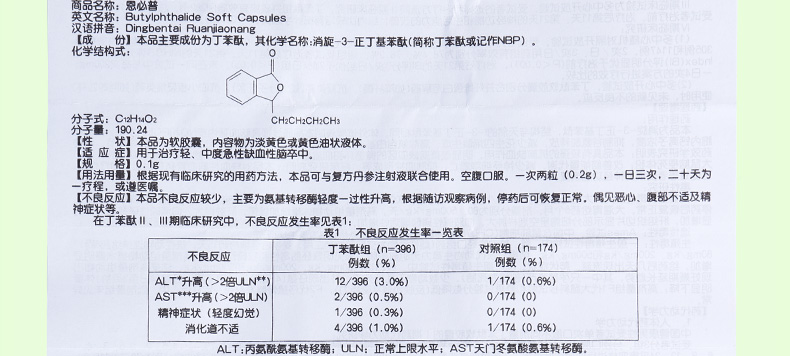
| 主要原料 | 本品主要成份为丁苯酞。 其化学名称:消旋-3-正丁基苯酞(简称丁苯酞或记作NBP) 分子式:C12H14O2 分子量:190.24 |
| 主要作用 | 用于治疗轻、中度急性缺血性脑卒中。 |
| 用法用量 | 根据现有临床研究的用药方法,本品可与复方丹参注射液联合使用。空腹口服,一次两粒(0.2g),一日三次,二十天为一疗程,或遵医嘱。 |
| 禁忌 | 下列患者禁用: 1.对本品或芹菜过敏者禁用。 2.有严重出血倾向者禁用。 |
| 注意事项 | 1.餐后服用影响药物吸收,建议餐前服用。 2.肝、肾功能受损者慎用。 3.用药过程中需要注意肝功变化。 4.因本品尚未进行出血性脑卒中临床研究,故不推荐出血性脑卒中患者使用。 5.有精神症状者慎用。 |
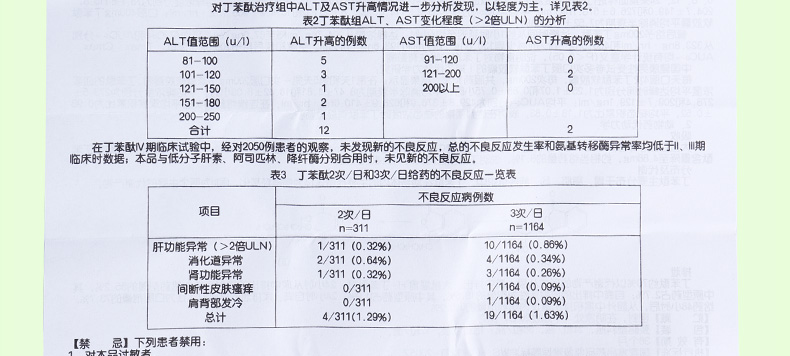
| 不良反应 | 本品不良反应较少, 主要为转氨酶轻度一过性升高, 根据随访观察病例, 停药后可恢复正常。 偶见恶心、 腹部不适及精神症状等。在丁苯酞Ⅱ 、 Ⅲ期临床研究中, 不良反应发生率见表 1:表 1 不良反应发生率一览表不良反应丁苯酞组(n=396)例数(%)对照组(n=174)例数(%)ALT 升高(>2×ULN)12/396 (3. 0%)1/174 (0. 6%)AST 升高(>2×ULN)2/396 (0. 5%)0/174 (0)精神症状(轻度幻觉)1/ 396 (0. 3%)0/174 (0)消化道不适4/ 396 (1. 0%)1/ 174 (0. 6)对丁苯酞治疗组中 ALT 及 AST 升高情况进一步分析发现, 以轻度为主, 详见表 2。表 2 丁苯酞组 ALT、 AST 变化程度(>2×ULN) 的分析 O O C H 2 C H 2 C H 2 C H 3 ALT 值范围(u /l)ALT 升高的例数AST 值范围(u /l)AST 升高的例数81-100101-120121-150151-180200-250合计5 3 1 2 1 1291-120121-200200 以上0202在丁苯酞 IV 期临床试验中, 经对 2050 例患者的观察, 未发现新的不良反应, 总的不良反应发生率和转氨酶异常率均低于 II、 III 期临床时数据; 恩必普与低分子肝素、 阿司匹林、 降纤酶分别合用时, 未见新的不良反应。表 3 丁苯酞 2 次/日和 3 次/日给药的不良反应一览表项目不良反应病例数2 次/日n=3113 次/日n=1164肝功能异常(>2×ULN)1/311(0. 32%)10/1164(0. 86%)消化道异常2/311(0. 64%)4/1164(0. 34%)肾功能异常1/311(0. 32%)3/1164(0. 26%)间断性皮肤瘙痒0/3111/1164(0. 09%)肩背部发冷0/3111/1164(0. 09%)总计4/311(1. 29%)19/1164(1. 63%) |
| 贮藏 | 密封,在阴凉处保存。 |
广东亮健药业有限公司-国家药监局认证的合法网上药店,致力于打造优质、低价、便捷的网上药店和最专业的健康服务平台
版权所有 Copyright©2006-2019 www.360lj.com All rights reserved


 进货单
进货单
